Probiotics vs periodontitis | First steps of periodontal biotherapy.
El uso de probióticos está muy extendido en el tratamiento de diversas infecciones y enfermedades sistémicas.
 |
| Dos probióticos inactivan a un patógeno periodontal. |
Probióticos en el control de las periodontitis. Importancia epidemiológica de conseguir nuevas alternativas terapéuticas en el control y tratamiento de las periodontitis.
La importancia de conseguir un tratamiento simple y efectivo de las periodontitis se deduce de la alta prevalencia de la misma. Los estudios epidemiológicos indican que entre el 13% y el 15% de las personas empiezan a presentar signos de periodontitis alrededor de los veinte años. A los treinta años puede llegar a un 60%, y a partir de los cincuenta años el 80% de las personas estarán afectadas.(1).
La periodontitis, además de provocar la pérdida de los dientes, también es un factor de riesgo de enfermedades como ictus, infecciones pulmonares, parto prematuro y bebés con bajo peso al nacer y disfunción eréctil vasculogénica entre otras. Por lo tanto, la necesidad de establecer una buena salud periodontal para lograr una buena salud sistémica trasciende el marco de la salud oral.
Etiopatogenia de las periodontitis que explican las limitaciones terapéuticas actuales.
En la medida que los dientes van erupcionando, en la superficie del esmalte se va formando y adhiriendo una biopelícula constituida principalmente por microorganismos que se extiende al margen gingival, y que si no se controla mediante la higiene oral provoca la forma más leve y frecuente de enfermedad periodontal que es la gingivitis.
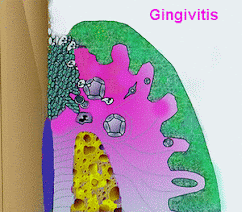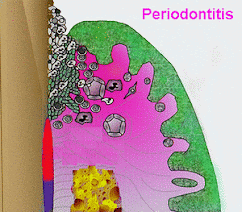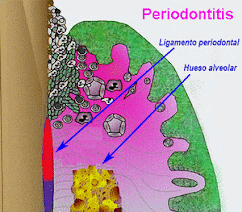 |
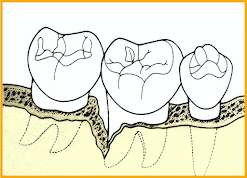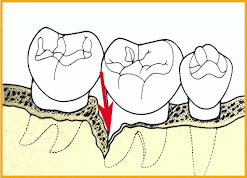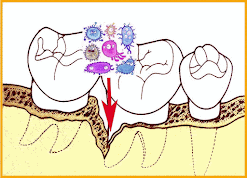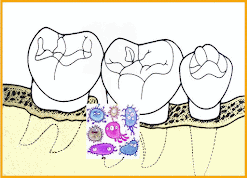
| Progresión de la gingivitis a periodontitis. Cambios más profundos que se producen en los tejidos. |
El nivel de acumulación de biopelícula, la virulencia de las bacterias que habitan en ella, y las respuestas inmunes humorales y celulares al microbioma de la biopelícula determinarán que la lesión se extienda y se desarrolle la periodontitis, que es la forma más progresiva y destructiva la cual afecta a todos los tejidos de soporte de los dientes, incluido el hueso alveolar (2-3).
El dibujo animado indica que lo cambios más profundos y significativos se producen en las periodontitis. Por ello, se representa el hueso en amarillo disminuido por la reabsorción, el ligamento periodontal dañado en rojo y con una mayor concentración de células de la inflamación.
 |
Recolonización de una bolsa periodontal después de ser tratada.. |
Los procedimientos terapéuticos actuales intentan eliminar mecánicamente la biopelícula del surco gingival, el sarro, el cemento necrótico de las raíces dentales expuestas por la destrucción ósea y la limpieza de las bolsas periodontales. Consisten en el desbridamiento subgingival (raspado y alisado radicular), las intervenciones quirúrgicas de limpieza profunda mediante colgajos, y el empleo coadyuvante de antisépticos y antibióticos puesto que con los procedimientos mecánicos no se pueden alcanzar todos los sitios e irregularidades del hueso y las raíces dentales. Por lo tanto, estos tratamientos no consiguen controlar la infección profunda definitivamente ya que con el tiempo se produce la recolonización de patógenos y se reactiva la periodontitis.
La administración de antibióticos sistémicos como tratamiento coadyuvante con la intención de controlar o reducir la carga microbiana patógena en los lugares no accesibles a la limpieza mecánica ha sido una alternativa durante décadas. Se han empleado cada vez más las combinaciones de antibióticos considerándose que estas son más eficaces. (Metronidazol, tetraciclinas, clindamicina, ciprofloxacina y amoxicilina han sido los más utilizados. (4).
Pero esto no es todo, ya que se emplean productos de aplicación profesional como el Atridox, consiste en colocar directamente 50 mg de doxiclina en el surco gingival mediante una cánula. Otra bomba contra las bacterias del microbioma oral es el Arestin, este es un sistema de microesferas de minociclina bioadhesivo y bioabsorbible que permiten la liberación sostenida de minociclina durante hasta 19 días. Con este sí que no quedan títeres con cabeza en el surco gingival, va dirigido a los patógenos, pero como estos no tienen un cartelito que los identifiquen fulmina de paso a los microorganismos de la microbiota. Ahora bien, no vaya a pensar el lector que con esto se cura la periodontitis, lo que se consigue, si acaso, son efímeras disminuciones de la profundidad de las bolsas periodontales. Con el tiempo vuelven a recolonizar los patógenos, y por supuesto son productos caros que necesitan varias visitas al dentista para recolocarlo. (No sólo dañan la microbiota oral sino el monedero).
Se ha informado que el uso crónico de antisépticos orales produce graves alteraciones del microbioma humano, en particular, las soluciones de clorhexidina. Se le denomina microbioma o microbiota al conjunto de todos los microorganismos (bacterias, arqueas, levaduras, eucariotas unicelulares, helmintos, hongos y virus ) que viven en nuestro interior como simbiontes. Este concepto fue postulado por Joshua Lederberg, Premio Novel de Medicina en 1958)
Este asunto es tan grave que se demostrado la asociación entre el uso crónico de clorhexidina con el desarrollo de enfermedades generales como diabetes, hipertensión etc. Recomiendo tanto a quienes los emplean como a los profesionales que los indican que revisen lo que hemos publicados en este portal.
En la modulación de la biología de los componentes microbianos, y no en provocar su disbiosis mediante agentes químicos, está el futuro. Hay que terminar con el uso de agentes químicos que, entre sus muchos inconvenientes, tiene el ser contaminantes medioambientales de difícil biodegradación como es el caso de la clorhexidina y el triclosán tan empleados en las formulaciones antisépticos orales para el "control de la biopelícula gingival".
Los antibióticos tampoco son la solución ya que no pueden eliminar todos los microorganismos patógenos (Campylobacter rectus subgingival, Porfiromona gingivalis, Treponema denticola, Tannerella forsythia y Aggregatibacter actinomycetemcomitans) y sólo consiguen reducir la concentración de uno de los patógenos más importantes que son los A. actinomycetemcomitans por lo que, en sujetos susceptibles, con el tiempo se recupera la concentración patógena y se reactiva la periodontitis. (5)
El uso de antibióticos en los tratamientos periodontales debe restringirse a casos muy seleccionados de una forma clínica particular que es la llamada periodontitis agresiva. No obstante, esto no siempre ocurre y muchas veces se indican ante cualquier tipo de periodontitis difícil de controlar.
 |
Bacteria feliz porque es resistente a los antibióticos. |
La utilización de antibióticos sistémicos es controvertida no sólo por su limitada eficacia sino también porque conduce al desarrollo de resistencia universal a los antimicrobianos. No todo el antibiótico va confinado a los tejidos periodontales, sino que por vía sanguínea se distribuye por todos los órganos y sistemas del cuerpo sin efectos positivos y solo efectos secundarios. El "precio" que paga la comunidad por el uso extensivo de los antibióticos en los tratamientos periodontales es el aumento de la resistencia bacteriana por lo que muchos antibióticos imprescindibles para controlar infecciones graves terminarán siendo inútiles.
Qué son los probióticos y cuáles son los más empleados.
 |
Elias Metchnikof. Nobel de Fisiologia 1908. |
En 2001, la OMS definió a los probióticos como microorganismos vivos que, administrados en cantidades adecuadas, brindan un beneficio en la salud más allá de la nutrición básica.
El término "probiótico" fue introducido en 1965 por Lilly & Stillwell y viene del griego y significa "de por vida” y es antónimo de "antibiótico". Al inicio del Siglo XX, el genial bacteriólogo ucraniano Iliá Metchnikoff, Premio Nobel de Fisiología y Medicina en 1908, quien desarrolló sus investigaciones en el Instituto Pasteur de París, expuso los fundamentos para el concepto de probióticos con una famosa investigación en la que sostenía que los búlgaros de una determinada región rural tenían una mayor longevidad debido a la leche fermentada que contiene bacterias viables y que publicó en un famoso libro titulado la Prolongación de la Vida. (Metchnikoff E. The prolongation of life. Journal of Dairy Science. 1907;36:356)
Se han detectado más de 700 especies de microorganismos formando parte de la microbiota de la boca humana. La flora normal (microbiota residente) de un individuo esta constituida por entre 30 y 100 especies de bacterias diferentes.(6).
 |
Bifidubacterium (los rosa) alternado con Lactobacillus. |
Los lactobacilos que se encuentran en la leche cruda y los productos lácteos fermentados como el queso, el yogur y la leche fermentada son omnipresentes en la dieta y se encuentran en el tracto gastrointestinal poco después del nacimiento (8).
Cómo funcionan los probióticos en el control de las periodontitis.
 |
| Soldado probiótico listo para la batalla. |
Se han propuesto varios mecanismos para explicar cómo funcionan los probióticos. Por ejemplo, estas bacterias secretan varias sustancias antimicrobianas tales como ácidos orgánicos, peróxido de hidrógeno y bacteriocinas, que son sustancias muy tóxicas para el metabolismo de los principales patógenos periodontales.
Otra forma importante de actuar de los probióticos es compitiendo con los microorganismos patógenos por los sitios de adhesión a la mucosa. Los probióticos también actúan modificando el entorno circundante, modulando el pH y / o el potencial de oxidación-reducción, lo que disminuye la eficacia patogénica de los microorganismos más virulentos. (9). Los probióticos detienen el desarrollo de la calcificación de la placa bacteriana disminuyendo la formación del sarro o cálculo, y lo que es especialmente importante en el caso de las periodontitis es que algunas cepas de probióticos (lactobacillus reuteri) pueden contribuir beneficiosamente al control de la destrucción del periodonto estimulando la inmunidad inespecífica y modulando la respuesta inmunitaria humoral y celular.(10-11).
El paradigma de la microbioterapia. Probióticos como nano soldados contra patógenos periodontales.
El tratamiento de la periodontitis tiene como objetivo fundamental el control de la infección bacteriana. Solo controlando la recolonización de los microorganismos patógenos es posible crear las condiciones que favorezcan la capacidad de los tejidos que forman el periodonto de autorepararse.
Como hemos visto anteriormente, esto solo se consigue parcialmente ya que se produce en más o menos tiempo la reinfección de los tejidos periodontales profundos. El uso de los probióticos, entre otros fundamentos, tiene provocar la recuperación del microbioma subgingival para que los microorganismo normales compitan con los patógenos como hemos visto anteriormente.
El fracaso del enfoque terapéutico actual está en que no conseguimos curar las periodontitis eliminando los microorganismos causales mediante agentes químicos o antibióticos. Esto en la práctica es imposible. Por tanto, es imperativo ante una enfermedad tan prevalente desarrollar nuevas estrategias terapéuticas, por ejemplo, la llamada recolonización guiada de las bolsas con probióticos, (13-14) que nos permitan controlar la progresión de las periodontitis con mayor eficacia sin usar antibióticos indiscriminadamente.
Aunque se dispone de varios estudios con resultados esperanzadores, cito al final del párrafo algunos de ellos, la trascendencia de controlar las periodontitis empleando bacterias normales adicionadas a la microbiota oral es de tal importancia epidemiológica que se necesitan más estudios aleatorizados y con muestras representativas que lo demuestren fehacientemente (12-30).
Formulaciones comerciales con probióticos destinados al tratamiento de las periodontitis.
 |
| Cápsula de probióticos. |
No todos los probióticos son iguales y los beneficios son dependientes de la elección de la cepa adecuada y la vía de administración. Las preparaciones de Lactobacillus están contraindicadas en personas con hipersensibilidad a la lactosa o la leche. S. boulardii está prohibido en pacientes con alergia a levaduras.
 |
Formas comercializadas de probióticos. |
Los resultados obtenidos hasta ahora por varios estudios que han introducido probióticos como nano soldados en el interior de las bolsas es alentador, ya que es una forma de establecer tratamientos más biológicos y eficientes que los antisépticos y antibióticos como coadyuvantes del tratamiento y control clínico de las periodontopatías.
Especialmente prometedores son los estudios de Tekce y col. (31) y de Quirynen M, (32) entre otros equipos de investigadores quienes han empleado el Lactobacilos reuteri en la recolonización de las bolsas periodontales.
El Lactobacilos reuteri se encuentra en la saliva y la placa subgingival, y evita el crecimiento excesivo de otros microorganismos patógenos. También reprime mediadores inflamatorios tales como factor de necrosis tumoral α, interleucina-8 y interleucina-1-β que contribuyen a la destrucción del periodonto de inserción.
Según la bióloga Lynn Margulis, a quien debemos las ideas fundamentales de un nuevo enfoque del origen de la vida en el planeta, la vida surgió de las bacterias hace entre 4000 y 5000 millones de años. Los organismos que no son bacterias han evolucionado a partir de organismos bacterianos. La vida es el extraño nuevo fruto de individuos que evolucionaron a partir de una simbiosis. Formamos parte de un ecosistema y también somos un ecosistema. Las bacterias hicieron posible la vida sobre la Tierra, y se unieron para crear la célula impulsando la evolución hacia organismos más complejos que dieron origen a los hongos, las plantas y los animales dentro de los que nos incluimos. "Solo en la actualidad hemos empezado a apreciar el hecho de que las bacterias son normales y necesarias para el cuerpo humano y que la salud no es un asunto tanto de destruir microrganismos como restablecer las apropiadas comunidades de bacterias" (Margulis y Sagan (33).
Por lo tanto, nuestro problema no es matar a las bacterias negando nuestro origen sino aprender a utilizarlas, y los probióticos orales son el más claro ejemplo de ello. ¿No será mas efectivo para controlar la periodontitis probiotizar las bolsas periodontales que intentar desesperadamente acabar con los microorganismos patógenos. ¿No será posible conseguir una simbiosis favorable para la salud periodontal entre patógenos periodontales y cepas probióticas. Les dejo la reflexión?. Todo es cuestión de tiempo y de ingeniería genética.
La rehabilitación del microbioma periodontal es el reto terapéutico para tratar y controlar las periodontitis eficaz y eficientemente. El uso de los probióticos es la alternativa más seductora que tenemos hasta ahora por su importancia ecológica y medio ambiental, bajo costo, carencia de efectos secundarios y facilidad de empleo. No tengo dudas, se está abriendo la puerta a un nuevo paradigma de tratamiento de la enfermedad periodontal y de una amplia gama de enfermedades usando como agentes terapéuticos nuestros propios microbios. La época de la microbioterapia no solo ha empezado sino que avanza a pasos agigantados.
Referencias bibliográficas.
2.Offenbacher S. Periodontal disease at the biofilm-gingival interface. Journal of Periodontology 2007;78:1911-1925.
3.Darveau RP. Periodontitis: A polymicrobial disruption of host homeostasis. Nature Reviews Microbiology. 2010;8:481-490.
4.Bidault P, Chandad F, Grenier D. Systemic antibiotic therapy in the treatment of periodontitis. J Can Dent Assoc. 2007;73(6):515-20.
5. Manas D, Srinivas SR, Jithendra KD. Role of antibiotics in periodontal therapy. Bangladesh J Med Sci. 2009;8(4):91-101.2).
6. Aas JA, Paster BJ, Stoles LN, Olsen I, Dewhirst FE. Defining the normal bacterial flora of the oral cavity. J Clin Microbiol 2005; 43: 5721-5732.
7. Suvarna VC, Boby VU. Probiotics in human health: A current assessment. Current Science 2005; 88: 1744- 1788.
8. Brunser O.T. El desarrollo de la microbiota intestinal humana, el concepto de probiótico y su relación con la salud humana. Rev. chil. nutr. vol.40 no.3 Santiago set. 2013.
8. Brunser O.T. El desarrollo de la microbiota intestinal humana, el concepto de probiótico y su relación con la salud humana. Rev. chil. nutr. vol.40 no.3 Santiago set. 2013.
9. Shetty A, Bhandary R, Thom.8 Aas B, Ramesh A, Hegde P. Probiotic significance in periodontics-A short review. IJDR 2017; 2(2); 57-60.
10. Simona G.., Neville G., Gibson R, Bartold M. Probiotics and Periodontitis – A Literature review. Journal of the International Academy of Periodontology 2017 19/2: 42–50.
11. Suvarna VC, Boby VU. Probiotics in human health: A current assessment. Current Science 2005; 88: 1744- 1788.
12. Magnusson I, Lindhe J, Yoneyama T and Liljenberg B. Recolonization of a subgingival microbiota following scaling in deep pockets. J. of Clinical Periodonl. 1984; 11:193-207.
13. Teughels W, Loozen G and Quirynen M. Do probiotics offer opportunities to manipulate the periodontal oral microbiota? Journal of Clinical Periodontology 2011; 38:159-177.
14. Teughels W, Newman MG, Coucke W, et al. Guiding periodontal pocket recolonization: A proof of concept. Journal of Dental Research 2007; 86:1078-1082.
15. Toiviainen A, Jalasvuori H, Lahti E, et al. Impact of orally administered lozenges with Lactobacillus rhamnosus GG and Bifi dobacterium animalis subsp. lactis BB-12 on the number of salivary mutans streptococci, amount of plaque, gingival infl ammation and the oral microbiome in healthy adults. Clinical Oral Investigations. 2015; 19:77-83.
13. Tripathi P, Dupres V, Beaussart A, et al. Deciphering the nanometer-scale organization and assembly of Lactobacillus rhamnosus GG pili using atomic force microscopy. Journal of Surfaces and Colloids 2012; 28:2211-2216.
14.Krasse P, et al. Decreased gum bleeding and reduced gingivitis by the probiotic Lactobacillus reuteri. Swedish Dental Journal. 2006;30:55-60. Probiotics and Periodontal Diseases. http://dx.doi.org/10.5772/intechopen.68814
15. Twetman S. Short-term effect of chewing gums containing probiotic Lactobacillus reuteri
on the levels of inflammatory mediators in gingival crevicular fluid. Acta Odontologica Scandinavica. 2009;67:19-24
16. Ince G, et al. Clinical and biochemical evaluation of lozenges containing Lactobacillus reuteri as an adjunct to non-surgical periodontal therapy in chronic periodontitis. Journal of Periodontology. 2015;86:746-754. DOI: 10.1902/jop.2015.140612
17. Vicario M, Santos A, Violant D, Nart J and Giner L. Clinical changes in periodontal subjects with the probiotic Lactobacillus reuteri Prodentis: A preliminary randomized clinical trial. Acta Odontologica Scandinavica. 2013; 71:813-819.
18. Vivekananda MR, Vandana KL and Bhat KG. Effect of the probiotic Lactobacilli reuteri (Prodentis) in the management of periodontal disease: a preliminary randomized clinical trial. Journal of Oral Microbiology. 2010; 2:1-9.
19. Yli-knuuttila H, Snäll J, Kari K and Meurman JH. Colonization of Lactobacillus rhamnosus GG in the oral cavity. Oral Microbiology and Immunology 2006; 21:129-13.
20. Iniesta M. Probiotic effects of orally administered Lactobacillus reuteri-containing tablets on the subgingival and salivary microbiota in patients with gingivitis. Journal of Clinical Periodontology. 2012;39:736-744. DOI: 10.1111/j.1600-051X.2012.01914.x.
21. Hallström H. Effect of probiotic lozenges on inflammatory reactions and oral biofilm during experimental gingivitis. Acta Odontologica Scandinavica. 2012;71:828-833.
22. Karuppaiah RM, et al. Evaluation of the efficacy of probiotics in plaque reduction and gingival health maintenance among school children—Control Trial. Journal of International Oral Health. 2013;5:33-37.
23. Purunaik S, Thippeswamy HM, Chavan SS. To evaluate the effect of probiotic mouth rinse on plaque and gingivitis among year old school children of Mysore, India. Randomized controlled trial. Global Journal of Medical Research. 2014;14:15-16.
24. Lee J, Kim SJ, Ko S, Ouwehand AC, Ma DS. Modulation of the host response by probiotic Lactobacillus brevis CD2 in experimental gingivitis. Oral Diseases. 2015;21:705-712.
25. Amižić IP, Cigić2 L, Gavić2 L, Radić M, Lukenda2 DB, Tonkić M, Barišić IG. Antimicrobial Efficacy of Probiotic-Containing Toothpastes: An in Vitro Evaluation. Med Glas (Zenica) 14 (1),139-144.2017 Feb 01.
26. Tekce M, Ince G, Gursoy H, Dirikan Ipci S, Cakar G, Kadir T, Yilmaz. S. Clinical and microbiological effects of probiotic lozenges in the treatment of chronic periodontitis: a 1-year follow-up study. J. Clin Periodontol 2015; 42: 363–372. doi: 10.1111/jcpe.12387.
27. Morales A, Galaz C, González J, Silva N, Hernández M, Godoy C, García-Sesnich J, Díaz P, Carvajal P. Efecto clínico del uso de probiótico en el tratamiento de la periodontitis crónica: ensayo clínico. Revista Clínica de Periodoncia, Implantología y Rehabilitación Oral, vol. 9, núm. 2, agosto, 2016, pp. 146-152.
28. Andon V, Arora V, Yadav V, Singh V, Punia H, Agrawal S, Gupta V. Concept of Probiotics in Dentistry. Int J Dent Med Res. 2015;1(6):206-209.
29. Zalba Elizari JI, Flichy-Fernández AJ. Empleo de probióticos en odontología. Nutr Hosp Vol. 28. Suplemento 1. 2013. 49-50.
30. Laleman I, Yilmaz E, Ozcelik O, Haytac C, Pauwels M, Herrero ER, Slomka V, Quirynen M, Alkaya B, Teughels W. The effect of a streptococci containing probiotic in periodontal therapy: a randomized controlled trial. J Clin Periodontol 2015; 42: 1032–1041. doi: 10.1111/jcpe.12464.
31. Gupta ND, Sharma S, Sharma VK. Probiotic – An emerging therapy in recolonizing periodontal pocket, J Oral Biol Craniofac Res. (2016), http://dx.doi.org/10.1016/j.jobcr.2016.09.002.
32. Quirynen M, Vogels R, Pauwels M. Initial subgingival colonization of 'pristine' pockets. J Dent Res. 2005;84(4):340–344.
33.Lynn Margulis / Dorion Sagan. Microcosmos. Editorial Tusquets, No. Ed 2013, pág. 7910. Simona G.., Neville G., Gibson R, Bartold M. Probiotics and Periodontitis – A Literature review. Journal of the International Academy of Periodontology 2017 19/2: 42–50.
11. Suvarna VC, Boby VU. Probiotics in human health: A current assessment. Current Science 2005; 88: 1744- 1788.
12. Magnusson I, Lindhe J, Yoneyama T and Liljenberg B. Recolonization of a subgingival microbiota following scaling in deep pockets. J. of Clinical Periodonl. 1984; 11:193-207.
13. Teughels W, Loozen G and Quirynen M. Do probiotics offer opportunities to manipulate the periodontal oral microbiota? Journal of Clinical Periodontology 2011; 38:159-177.
14. Teughels W, Newman MG, Coucke W, et al. Guiding periodontal pocket recolonization: A proof of concept. Journal of Dental Research 2007; 86:1078-1082.
15. Toiviainen A, Jalasvuori H, Lahti E, et al. Impact of orally administered lozenges with Lactobacillus rhamnosus GG and Bifi dobacterium animalis subsp. lactis BB-12 on the number of salivary mutans streptococci, amount of plaque, gingival infl ammation and the oral microbiome in healthy adults. Clinical Oral Investigations. 2015; 19:77-83.
13. Tripathi P, Dupres V, Beaussart A, et al. Deciphering the nanometer-scale organization and assembly of Lactobacillus rhamnosus GG pili using atomic force microscopy. Journal of Surfaces and Colloids 2012; 28:2211-2216.
14.Krasse P, et al. Decreased gum bleeding and reduced gingivitis by the probiotic Lactobacillus reuteri. Swedish Dental Journal. 2006;30:55-60. Probiotics and Periodontal Diseases. http://dx.doi.org/10.5772/intechopen.68814
15. Twetman S. Short-term effect of chewing gums containing probiotic Lactobacillus reuteri
on the levels of inflammatory mediators in gingival crevicular fluid. Acta Odontologica Scandinavica. 2009;67:19-24
16. Ince G, et al. Clinical and biochemical evaluation of lozenges containing Lactobacillus reuteri as an adjunct to non-surgical periodontal therapy in chronic periodontitis. Journal of Periodontology. 2015;86:746-754. DOI: 10.1902/jop.2015.140612
17. Vicario M, Santos A, Violant D, Nart J and Giner L. Clinical changes in periodontal subjects with the probiotic Lactobacillus reuteri Prodentis: A preliminary randomized clinical trial. Acta Odontologica Scandinavica. 2013; 71:813-819.
18. Vivekananda MR, Vandana KL and Bhat KG. Effect of the probiotic Lactobacilli reuteri (Prodentis) in the management of periodontal disease: a preliminary randomized clinical trial. Journal of Oral Microbiology. 2010; 2:1-9.
19. Yli-knuuttila H, Snäll J, Kari K and Meurman JH. Colonization of Lactobacillus rhamnosus GG in the oral cavity. Oral Microbiology and Immunology 2006; 21:129-13.
20. Iniesta M. Probiotic effects of orally administered Lactobacillus reuteri-containing tablets on the subgingival and salivary microbiota in patients with gingivitis. Journal of Clinical Periodontology. 2012;39:736-744. DOI: 10.1111/j.1600-051X.2012.01914.x.
21. Hallström H. Effect of probiotic lozenges on inflammatory reactions and oral biofilm during experimental gingivitis. Acta Odontologica Scandinavica. 2012;71:828-833.
22. Karuppaiah RM, et al. Evaluation of the efficacy of probiotics in plaque reduction and gingival health maintenance among school children—Control Trial. Journal of International Oral Health. 2013;5:33-37.
23. Purunaik S, Thippeswamy HM, Chavan SS. To evaluate the effect of probiotic mouth rinse on plaque and gingivitis among year old school children of Mysore, India. Randomized controlled trial. Global Journal of Medical Research. 2014;14:15-16.
24. Lee J, Kim SJ, Ko S, Ouwehand AC, Ma DS. Modulation of the host response by probiotic Lactobacillus brevis CD2 in experimental gingivitis. Oral Diseases. 2015;21:705-712.
25. Amižić IP, Cigić2 L, Gavić2 L, Radić M, Lukenda2 DB, Tonkić M, Barišić IG. Antimicrobial Efficacy of Probiotic-Containing Toothpastes: An in Vitro Evaluation. Med Glas (Zenica) 14 (1),139-144.2017 Feb 01.
26. Tekce M, Ince G, Gursoy H, Dirikan Ipci S, Cakar G, Kadir T, Yilmaz. S. Clinical and microbiological effects of probiotic lozenges in the treatment of chronic periodontitis: a 1-year follow-up study. J. Clin Periodontol 2015; 42: 363–372. doi: 10.1111/jcpe.12387.
27. Morales A, Galaz C, González J, Silva N, Hernández M, Godoy C, García-Sesnich J, Díaz P, Carvajal P. Efecto clínico del uso de probiótico en el tratamiento de la periodontitis crónica: ensayo clínico. Revista Clínica de Periodoncia, Implantología y Rehabilitación Oral, vol. 9, núm. 2, agosto, 2016, pp. 146-152.
28. Andon V, Arora V, Yadav V, Singh V, Punia H, Agrawal S, Gupta V. Concept of Probiotics in Dentistry. Int J Dent Med Res. 2015;1(6):206-209.
29. Zalba Elizari JI, Flichy-Fernández AJ. Empleo de probióticos en odontología. Nutr Hosp Vol. 28. Suplemento 1. 2013. 49-50.
30. Laleman I, Yilmaz E, Ozcelik O, Haytac C, Pauwels M, Herrero ER, Slomka V, Quirynen M, Alkaya B, Teughels W. The effect of a streptococci containing probiotic in periodontal therapy: a randomized controlled trial. J Clin Periodontol 2015; 42: 1032–1041. doi: 10.1111/jcpe.12464.
31. Gupta ND, Sharma S, Sharma VK. Probiotic – An emerging therapy in recolonizing periodontal pocket, J Oral Biol Craniofac Res. (2016), http://dx.doi.org/10.1016/j.jobcr.2016.09.002.
32. Quirynen M, Vogels R, Pauwels M. Initial subgingival colonization of 'pristine' pockets. J Dent Res. 2005;84(4):340–344.
